Luând știința în propriile mâini. Cum încearcă familiile să îi salvează pe cei dragi de boli rare


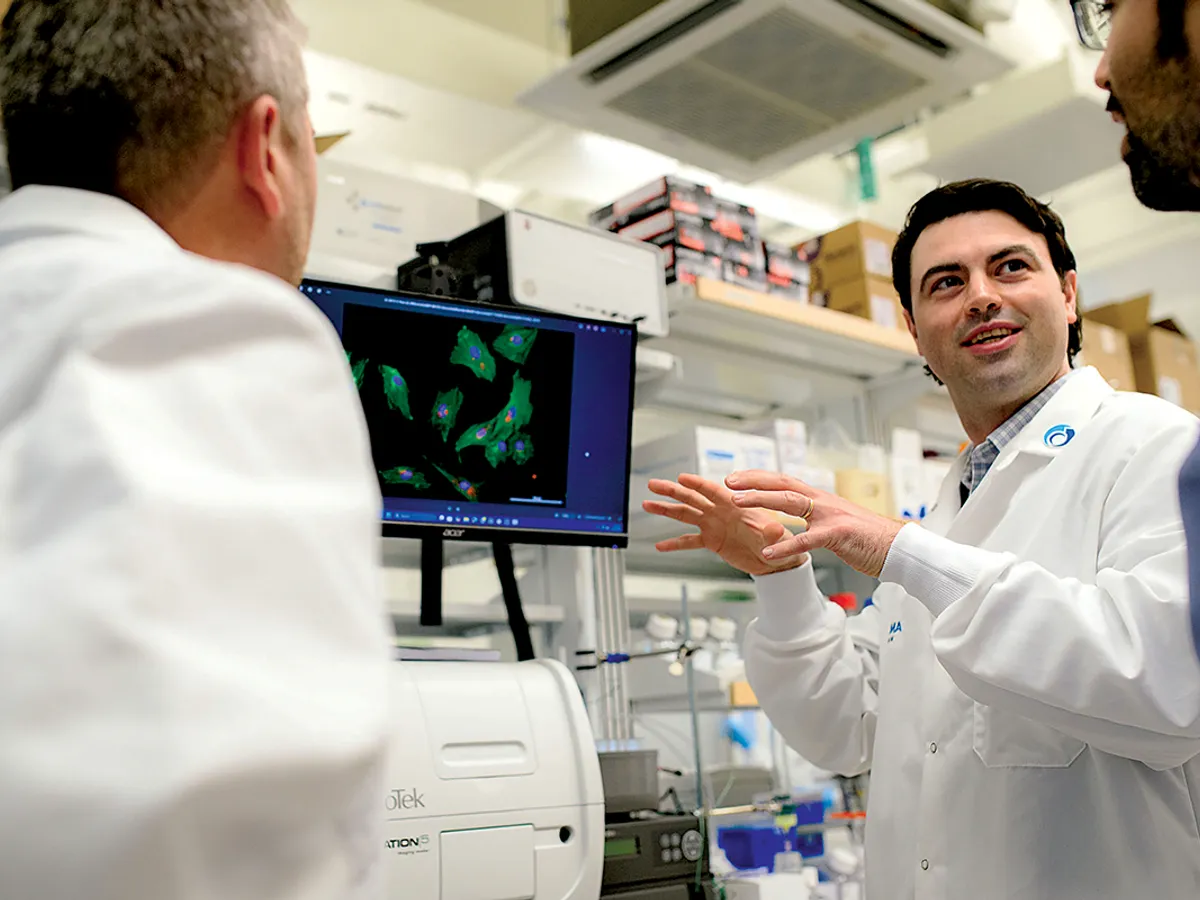
În cursa pentru tratarea bolilor rare, familiile sunt în fruntea eforturilor de a găsi singure leacuri.
Când Casey McPherson a devenit tată, scopul său a devenit clar. Trebuia să-și crească fiica, Rose, pentru a fi iubitoare, curajoasă, sănătoasă și puternică. Trebuia să o protejeze.
Așadar, când neurologul pediatru i-a spus lui McPherson că Rose avea o boală genetică rară, atât de neobișnuită încât nici măcar nu avea un nume, instinctul părintesc a intrat în acțiune. Iar când medicul i-a spus: „Nu putem face nimic“, instinctul acela s-a accentuat.
„Rose era atacată, dar nu era niciun monstru pe care să-l pot ucide și nicio mașină în fața căreia să mă arunc“, a declarat McPherson pentru Newsweek.
„Era doar un singur nucleotid în genă. Și dacă acela era monstrul pe care trebuia să-l omor, atunci acela era monstrul pe care îl urmăream“.
Rose, acum în vârstă de 9 ani, și McPherson, 46 de ani, luptă împotriva acelei boli „monstruoase“ în fiecare zi, cu mici gesturi. Casa lor din suburbia orașului Austin, din Texas, este „Rosie-proof“, după cum spune McPherson.
Ea doarme într-un pat special echipat cu bariere pentru a o împiedica să se rătăcească, iar o cameră video și monitoare de oxigen și puls scanează semne de crize în timpul nopții. Rose nu are restricțiile unui copil de 9 ani neurotipic, așa că substanțele chimice și aparatele electronice sunt păstrate în spatele a trei serii de încuietori.
Ea ia medicamente pentru convulsii de două ori pe zi și merge la o școală privată pentru copii cu nevoi speciale (plătită din buzunarul propriu, deoarece exista o listă de așteptare de 15 ani pentru orice fel de asistență financiară).
„Rose era atacată, dar nu era
niciun monstru pe care să-l
pot ucide și nicio mașină în fața
căreia să mă arunc. Era doar
un singur nucleotid în genă“
Înainte, McPherson era cunoscut ca solistul trupelor de rock alternativ Alpha Rev și Flying Colors. După diagnosticul lui Rose, în 2016, el a preluat un nou rol ca fondator, lansând fundația non-profit To Cure a Rose Foundation, organizația de cercetare contractuală Everlum Bio și, acum, corporația de utilitate publică Alpha-Rose Therapeutics.
Toate trei caută să găsească și să finanțeze tratamente pentru copiii cu boli genetice extrem de rare, precum cea a lui Rose.
McPherson face parte dintr-un grup tot mai mare de părinți, soți și pacienți care caută tratamente pentru boli rare. Mulți dintre ei nu sunt oameni de știință sau medici.
Dar, după cum au declarat mulți pentru Newsweek, tocmai asta este avantajul lor. Cercetarea științifică este compartimentată, lentă și împovărată de birocrație. Cei care înțeleg complexitatea medicinei consideră că anumite proiecte de cercetare sunt imposibile. Cei care au un apropiat cu o boală rară nu văd altă opțiune. Ei nu acceptă un „nu“ sau cuvântul „încet“ ca răspuns.
De ce pacienții cu boli rare intră în arena cercetării?
În Statele Unite, între 25 și 30 de milioane de americani trăiesc cu o boală rară, potrivit Institutului Național de Sănătate (NIH). Există peste 10.000 de boli rare cunoscute și, împreună, acestea afectează unu din zece americani. Fiecare afecțiune reprezintă doar un segment mic al populației, dar, combinate, acestea afectează o parte semnificativă.
O boală rară este clasificată ca fiind una care afectează mai puțin de 200.000 de americani. Unele afectează doar câteva sute de persoane, ceea ce face dificilă obținerea de fonduri limitate pentru cercetare și completarea studiilor clinice.
„Dacă abordăm o singură boală la un moment dat, ținând cont de calendarul de dezvoltare a medicamentelor, vor trece generații întregi până când vom avea un număr substanțial de tratamente“, a declarat pentru Newsweek, dr. Dominique Pichard, directorul Diviziei de Cercetare și Inovare în Domeniul Bolilor Rare din cadrul Centrului Național pentru Avansarea Științelor Translaționale al NIH. Mai puțin de 5% dintre bolile rare cunoscute au tratamente aprobate de FDA.
„Ghinionul... a devenit
un scop, acela de a
transforma durerea
ei în ceva“
„Trebuie să găsim modalități mai bune de a rezolva problema accesului la tratamente pentru acești pacienți“, a subliniat Pichard.
În cadrul NCATS, Pichard lucrează la crearea de oportunități de finanțare care să rezolve unele dintre aceste provocări. Ea își propune să adopte o „abordare de platformă“ a cercetării în domeniul bolilor rare, similară celei utilizate în oncologie. Cancerul în sine nu este considerat rar, dar multe tipuri de cancer sunt rare.
Dacă cercetătorii din domeniul oncologiei ar fi analizat câte un subtip pe rând, progresele ar fi fost lente, dar prin gruparea tipurilor de cancer și vizarea căilor comune, ei au multiplicat impactul fiecărei investiții.
Pichard speră să reproducă acest tip de cadru adaptabil, independent de boală, în cercetarea bolilor rare. Afecțiunile cu denumiri și manifestări diferite pot avea totuși mecanisme biologice comune. Dacă aceste legături sunt descoperite, resursele limitate ar putea fi extinse pentru a deservi pacienții cu afecțiuni rare multiple.

PERANȚĂ McPherson cu fiicele sale Weston și Rose
Grupurile de susținere a pacienților au devenit din ce în ce mai importante pentru această activitate. Ele pun bazele unei abordări de tip platformă prin organizarea datelor, strângerea de fonduri pentru cercetare, educarea medicilor și chiar reunirea oamenilor de știință pentru a demara procesul. Platformele de socializare și sistemele de videoconferință au facilitat mobilizarea pacienților din toată țara.
„Recunoaștem cât de important este ca pacienții sau organizațiile de pacienți să fie implicați în cercetare, deoarece ei cunosc realitatea acestor afecțiuni“, a spus Pichard. Pentru mulți apărători ai drepturilor pacienților, această discrepanță între înțelegerea științifică a bolii și propria experiență de viață este ceea ce îi motivează.
Cum contribuie apărătorii drepturilor pacienților la progresul cercetării?
Jeanne Whiting și Marlene Portnoy sunt cofondatoarele Fundației pentru Cercetarea Tumorilor Desmoide, care sărbătorește anul acesta 20 de ani de existență. Whiting a fost diagnosticată cu o tumoare desmoidă în 2001. După ce soțul lui Portnoy a fost diagnosticat în 2004, cele două femei din New Jersey s-au cunoscut pe o listă de discuții și au decis să înființeze o fundație. Râzând, Whiting a numit această decizie ca fiind „naivă“.
Dar nu existau multe alte speranțe, au declarat ele pentru Newsweek. Portnoy își amintește că a călătorit împreună cu soțul ei la patru instituții medicale diferite după un an de diagnostice eronate. Fiecare i-a dat un protocol diferit și i-a spus că nu știe prea multe despre boală, „ceea ce este o experiență cu adevărat terifiantă“, a spus ea.
Doar aproximativ 1% din cazurile de cancer sunt sarcoame, iar în acest procent se regăsesc peste 70 de subtipuri. Deși tumorile desmoide sunt legate de sarcoamele țesuturilor moi și sunt tratate de medici oncologi, ele afectează doar între doi și patru pacienți la un milion, astfel încât mulți medici nu sunt pregătiți să le trateze.
Whiting și Portnoy au devenit organizația și vocea principală pentru această afecțiune prin activitatea fundației lor, organizând gale de strângere de fonduri și ateliere anuale pentru medici și pacienți. Au adunat experți pentru a redacta primul document de consens privind tumorile desmoide: un acord pentru standardizarea înțelegerii în cadrul comunității medicale, care include un algoritm pentru personalizarea tratamentului în cazurile sensibile.
„Eram două femei la masa din bucătărie, dar nu ne-a fost frică să punem întrebări“, a spus Portnoy.
Una dintre cele mai importante realizări ale lor a fost în noiembrie 2023, când Food and Drug Administration a aprobat primul medicament pentru tumorile desmoide. Nu a fost o călătorie ușoară. Încă din 2010, Portnoy și Whiting coordonau cercetătorii, NIH, Pfizer și SpringWorks Therapeutics pentru a accelera dezvoltarea medicamentului. La un moment dat, Pfizer a decis să întrerupă dezvoltarea, dar fondatoarele fundației au continuat să insiste.
„Am continuat să sunăm și să sunăm și să sunăm“, a spus Portnoy. Dacă nu ar fi făcut-o, medicamentul ar fi putut să nu ajungă niciodată la pacienți.
Fundația Chordoma promovează descoperirile pentru pacienții cu forme rare de cancer
Josh Sommer cunoaște bine acest tip de perseverență. În 2006, era student la inginerie la Universitatea Duke când a fost diagnosticat cu cordom, un sarcom osos rar care afectează coloana vertebrală și baza craniului, diagnosticat la una dintr-un milion de persoane în fiecare an.
Cordomul era puțin cunoscut și nu exista niciun tratament disponibil în afară de chirurgie și radioterapie la momentul diagnosticării. Perioada medie de supraviețuire a pacienților era de aproximativ opt ani după diagnosticare.
„La 18 ani, era o statistică destul de dificil de acceptat“, a declarat Sommer pentru Newsweek, „și, pentru a scurta povestea, m-am hotărât să fac tot posibilul pentru a schimba aceste șanse“.
Fără „niciun bagaj util, în afară de mult entuziasm și o înclinație spre știință“, Sommer își amintește că a găsit singurul cercetător din afara NIH care lucra la această boală. În mod ironic, laboratorul său se afla tot la Duke, iar lui Sommer i s-a oferit un post. Dar nu aveau acces la modele de șoareci, țesut tumoral, linii celulare și nu aveau nici fonduri suficiente. În plus, lucrau în izolare completă, așa că progresul era lent.
„Dacă nu studiezi un model fiabil al bolii, rezultatele nu vor duce la tratamente mai bune“, a spus Sommer. „De fapt, ar putea avea efectul opus. Așadar, era foarte evident că domeniul nu se autocorecta și nu rezolva singur această problemă“.
În jurul anului 2008, Sommer a înființat Fundația Chordoma, cu scopul de a crea condițiile adecvate pentru o cercetare semnificativă. De atunci, fundația a contribuit la introducerea a peste o duzină de terapii în studiile clinice și a inițiat eforturi de descoperire pentru a dezvolta medicamente care vizează o genă cunoscută drept „călcâiul lui Ahile“ al cordomului.
Cum grupurile de advocacy stimulează recrutarea pentru studiile clinice
Una dintre barierele în calea cercetării bolilor rare este recrutarea pentru studiile clinice. În cercetarea pentru medicamentul împotriva tumorii desmoide, Institutul Național al Cancerului a estimat că ar fi nevoie de ani de zile pentru a completa un studiu, având în vedere rata scăzută de diagnosticare.
Dar, datorită conexiunilor Fundației pentru Cercetarea Tumorilor Desmoide, studiul a fost completat în mai puțin de cinci luni. Jeanette Cesta, director executiv al Fundației VWD Connect pentru boala von Willebrand severă (o boală ereditară rară care provoacă sângerări), a observat o schimbare în comunicarea cu companiile de cercetare.
„Acum, când se caută noi produse pentru VWD, ne contactează“, a declarat Cesta pentru Newsweek. „Aceste companii își dau seama că, dacă nu înțeleg experiența pacientului și nu înțeleg ce este important pentru acesta, nu vor reuși niciodată să-l motiveze să participe la studiul clinic“, a spus ea.
Implicarea oamenilor de știință în relația cu pacienții este un pas înainte, dar nu garantează participarea la cercetarea bolilor rare. Potrivit unui raport al NIH din 2024, mai puțin de 10% dintre persoanele cu scleroză laterală amiotrofică (SLA), o boală rară a sistemului nervos, participă la studii clinice.
Siddu Tummala, directorul general al unei companii de date și analize din Texas, a fost diagnosticat cu SLA în primăvara anului 2024.
El a vorbit despre impactul emoțional pe care îl are auzirea unui medic care spune „nu există leac“ și conștientizarea faptului că studiul nu are șanse să-l salveze de prognosticul nefavorabil al SLA. Majoritatea pacienților supraviețuiesc între doi și cinci ani după diagnostic, pierzând controlul asupra mușchilor pe măsură ce boala neurodegenerativă progresează. Deși pacienții ar dori să contribuie la binele comun, Tummala a spus că „este posibil ca în acest moment să nu aibă mentalitatea necesară“.
Tummala a relatat supărarea colectivă a colegilor săi pacienți, care știu că cercetarea se va întinde pe zeci de ani, pe care ei nu se așteaptă să-i mai trăiască.
Care sunt dezavantajele apărării drepturilor pacienților?
La NCATS, Pichard lucrează pentru a educa comunitatea de pacienți cu privire la procesul de dezvoltare a medicamentelor și de cercetare clinică, organizând ateliere și creând resurse, cum ar fi Toolkit for Patient-Focused Therapy Development (Setul de instrumente pentru dezvoltarea terapiei centrate pe pacient), un ghid cuprinzător care ajută la parcurgerea procesului complicat de cercetare și dezvoltare.
Fundațiile în sine se concentrează, de asemenea, pe reducerea caracterului intimidant al studiilor clinice. La Chordoma Foundation, Sommer consideră că navigatorii pentru pacienți sunt factori de schimbare.
Aceștia petrec ore întregi însoțind pacienții în procesul de înscriere în studiile clinice.
Dar nu există navigatori pentru pacienții și familiile care fac primul pas în necunoscut, aventurându-se în lumea complexă a scrierii de cereri de finanțare și a finanțării NIH. Deși găsesc sprijin pe parcurs, mulți apărători ai pacienților se confruntă cu sindromul impostorului în timp ce lucrează la construirea organizațiilor lor.
Unii primesc chiar respingere din partea profesioniștilor.
„Mi s-a spus: «Ești un apărător al pacienților. Rămâi la locul tău»“, a spus McPherson. „Dar ceea ce m-a motivat a fost Rose“.
Eforturile lui McPherson dau roade. AlphaRose Therapeutics a strâns 1,1 milioane de dolari din ianuarie pentru a angaja o echipă de experți care utilizează cercetarea în domeniul AI pentru a dezvolta tratamente pentru mutații genetice și boli rare. Recent, el a vizitat Capitol Hill pentru a pleda în favoarea pacienților cu boli rare. În Congres au fost introduse mai multe proiecte de lege privind bolile rare, cu scopul de a simplifica și stimula procesul de descoperire a medicamentelor pentru afecțiuni rare.
„A început ca o misiune de a o vindeca pe Rosie, dar mi-am dat seama că Rosie mi-a dat misiunea de a schimba viețile multor alți copii“, a spus el. „O mână proastă care i-a fost împărțită ei și familiei noastre a devenit un scop, acela de a transforma durerea ei în ceva“.
El speră că, peste ani, o altă fetiță și tatăl ei vor intra într-o clinică, iar medicul le va spune: „Avem un medicament pentru voi“.
Alexis Kayser este redactorul secțiunii de sănătate al revistei Newsweek. O puteți contacta prin e-mail la adresa [email protected]

















